Los tampones no volátiles como el fosfato y el citrato son generalmente incompatibles con la detección espectrométrica de masas (LC-MS) o causan una interferencia significativa con la generación de iones. En el caso de los caudales de HPLC convencionales, la deposición continua de tampón provoca el encresamiento de la fuente de iones del espectrómetro de masas, que puede degradar el rendimiento de la interfaz LC/MS.
La LC-MS (cromatografía líquida-espectrometría de masas) es una técnica analítica en química que combina las capacidades de separación física de la LC con las capacidades de la MS. La cromatografía líquida de alto rendimiento separa las mezclas de muestras de moléculas y la espectrometría de masas proporciona una identificación estructural de cada molécula con alta sensibilidad de detección y especificidad molecular.
Se sugiere que el tampón fosfato debe evitarse en la fase móvil del análisis LC-MS debido a su baja volatilidad. Pasan una gran cantidad de tampones en la ESI que son complicados de eliminar y se forman grandes cantidades de sal en la EM. Éste es el motivo principal para evitar este tipo de buffer. Si su analito contiene un grupo fosfato, éste no es el problema, porque utilizamos la concentración de analito en nanogramos. Puede utilizar el ácido trifluoroacético (TFA) como alternativa al tampón, ya que es ácido y volátil.
La fase móvil debe ser volátil cuando se utiliza un espectrómetro de masas como detector de cromatografía líquida, ya que una de las funciones de la interfaz LC-MS es vaporizar la fase móvil. El principal problema es que el tampón fosfato no es volátil y, por tanto, no se puede utilizar en experimentos LC-MS.
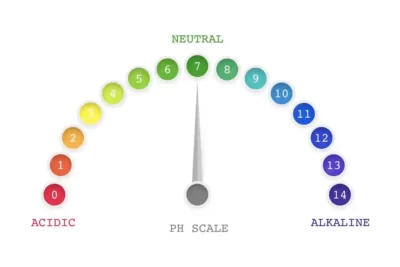
Existen opciones limitadas de búfer disponibles para LC-MS porque el búfer debe ser volátil a las aplicaciones de LC-MS. Los tampones LC-MS más comunes son el acetato, el formiato, el amoníaco y el bicarbonato, etc. El análisis de analitos en los intervalos de pH 2,0 a 3,8 y pH de 5,8 a 8,0 normalmente se realiza con acetato de amonio. El análisis de los analitos en los intervalos de pH de 2,7 a 3,7 normalmente se realiza con formado de amonio. El análisis de compuestos en los intervalos de pH de 6,6 a 8,6 normalmente se realiza con bicarbonato de amonio. Estos no cubren completamente el rango de búfer requerido, pero son la única opción para aplicaciones LC-MS.



Deja una respuesta