Que diferencia principal entre la resonancia y la conjugación π es que La resonancia se refiere a la estabilidad de una molécula en presencia de electrones deslocalizados, mientras que la conjugación π se refiere al concepto de que los electrones pi se distribuyen por toda el área de una molécula y no pertenecen a un solo átomo en la molécula..
La resonancia y la conjugación π son términos estrechamente relacionados, ya que la conjugación π provoca resonancia en los compuestos químicos.
CONTENIDO
1. Descripción general y diferencia clave
2. ¿Qué es la resonancia?
3. ¿Qué es la conjugación π?
4. Comparación lado a lado: resonancia frente a conjugación π en forma tabular
5. Resumen
¿Qué es la resonancia?
La resonancia es un concepto químico que describe la interacción entre pares de electrones solitarios y pares de electrones de enlace en un compuesto. En general, el efecto de la resonancia es útil para determinar la estructura química real de ese compuesto orgánico o inorgánico. Este efecto también ocurre en compuestos químicos que contienen dobles enlaces y pares de electrones solitarios. Además, este efecto provoca la polaridad de las moléculas.
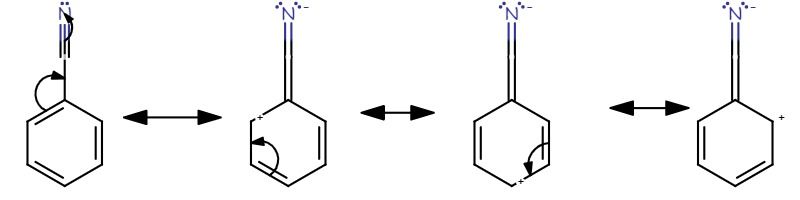
La resonancia muestra la estabilización de un compuesto químico por deslocalización de electrones en enlaces pi. Los electrones en las moléculas pueden moverse alrededor de los núcleos atómicos porque un electrón no tiene un lugar fijo dentro del átomo. Por lo tanto, los pares de electrones solitarios pueden pasar a enlaces pi y viceversa. Esto se hace para lograr un estado estacionario. Este proceso de movimiento de electrones se llama resonancia. Además, podemos usar estructuras de resonancia para obtener la estructura más estable de una molécula.

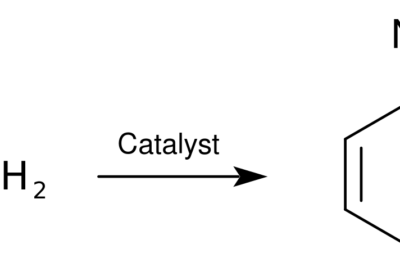
Figura 01: Resonancia en benzonitrilo.
Una molécula puede tener múltiples estructuras de resonancia según el número de pares solitarios y enlaces pi presentes en esa molécula. Todas las estructuras de resonancia de una molécula tienen el mismo número de electrones y la misma disposición de átomos. La estructura real de esta molécula es una estructura híbrida en todas las estructuras de resonancia. Hay dos tipos de efectos de resonancia: efectos de resonancia positivos y efectos de resonancia negativos.
El efecto de resonancia positiva explica la resonancia que se encuentra en los compuestos cargados positivamente. El efecto de resonancia positiva ayuda a estabilizar la carga positiva en esta molécula. El efecto de resonancia negativa explica la estabilización de una carga negativa en una molécula. Sin embargo, la estructura híbrida obtenida considerando la resonancia tiene menor energía que todas las estructuras de resonancia.
¿Qué es la conjugación de π?
El término conjugación π se refiere a la deslocalización en compuestos orgánicos donde podemos observar la distribución de electrones pi no enlazantes a través de una molécula. Por lo tanto, podemos describir los electrones en un sistema de conjugación π como los electrones no enlazantes en ese compuesto químico. Además, este término se refiere a los electrones que no están unidos a un solo átomo o enlace covalente.
Como ejemplo simple, podemos dar el benceno como un sistema aromático con electrones deslocalizados. En general, un anillo de benceno tiene seis electrones pi en la molécula de benceno; A menudo los indicamos gráficamente con un círculo. Este círculo significa que todos los átomos en la molécula tienen electrones pi asociados con ellos. Esta deslocalización hace que el anillo de benceno tenga enlaces químicos con longitudes de enlace similares.
¿Cuál es la diferencia entre resonancia y conjugación π?
La conjugación de resonancia y pi son términos estrechamente relacionados. los diferencia principal entre la resonancia y la conjugación π es que la resonancia se refiere a la estabilidad de una molécula en presencia de electrones deslocalizados, mientras que la conjugación π se refiere al concepto de que los electrones pi están y no están distribuidos en toda el área de un molécula pertenecen a un solo átomo en la molécula.
Resumen: resonancia frente a conjugación π
La resonancia y la conjugación π son términos estrechamente relacionados en los que la conjugación π provoca la resonancia en los compuestos químicos. los diferencia principal entre la resonancia y la conjugación π es que la resonancia se refiere a la estabilidad de una molécula en presencia de electrones deslocalizados, mientras que la conjugación π se refiere al concepto de que los electrones pi están y no están distribuidos en toda el área de un molécula pertenecen a un solo átomo en la molécula.
Relación:
1. "Conjugación y resonancia en química orgánica". Maestría Química Orgánica26 de enero de 2020, disponible aquí.
Imagen de cortesía:
1. "Resonancia de benzonitrilo" por Fung06831 - Trabajo propio (CC BY-SA 4.0) a través de Commons Wikimedia